PROBLEMA
Studio della terza variabile prevista dalla
nostra ipotesi di lavoro: la sostanza
IPOTESI (costruzione)
Abbiamo provato
ad eseguire un esperimento con la sostanza rame a temperatura ambiente e l'acqua più o meno calda, abbiamo determinato la
temperatura finale del miscuglio e ci siamo accorti che le nostre previsioni aritmetiche
non funzionavano più.
Qualcuno di noi
sostiene che ci deve essere una costante per quella sostanza e che occorre individuarla in
quanto se non c’è calore disperso nell’ambiente, grazie ai contenitori e ai i
tempi brevi dell'esperimento, la quantità ceduta da una massa deve essere quella
assorbita dall’altra nei limiti della precisione sperimentale.
Come si può
procedere?
Studenti:
il rame si scalda prima e quindi avrà una necessità di calore diversa rispetto
all'acqua, perché è un metallo.
Prof.ssa: ma nella nostra formula questo non compare; proviamo a
lavorare sulla formula.
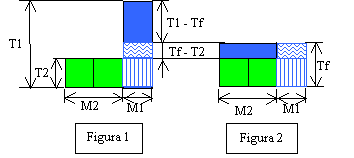
Disegniamo di nuovo i
nostri modellini (vedi relazione n.3)
Come si vede
dalle parti in blu, la differenza di temperatura finale e iniziale per massa1 è uguale
alla differenza di temperatura iniziale e finale per massa2
Studente: allora si può scrivere una nuova formula:
differenza1 x massa1 =
differenza2 x massa2
Prof.ssa:
sfruttiamo questa formula per eseguire un esperimento. Se i due prodotti non
coincidono……
Studenti:
se...
Calcoliamo i prodotti
250 . (64 -
24) = 10000
250
. (70 - 64) = 1500
Prof.ssa:poiché i due
prodotti non sono uguali dipenderà dal rame…
Studente: allora troviamo per
quale valore deve essere moltiplicato il 10000 per ottenere 1500, cioè 1500 : 10000 =
0,15
Prof.ssa: se questo
valore è costante, nel limite degli errori sperimentali, avremo trovato che il rame ha
una costante che riguarda il calore e che per ora chiamiamo costante del rame.
PROCEDIMENTO
Abbiamo preso una
quantità di acqua calda e l’abbiamo immersa in un contenitore di polistirolo con
dentro delle sbarrette di rame. Per determinare la temperatura del rame misuravamo la
temperatura dell'aria circostante il rame nel contenitore già predisposto.
L’esperimento riportato presenta i dati ottenuti con il rame
trattato alla fiamma prima di essere utilizzato per l’esperimento.
| M1(g) |
M2 (g) |
T1 (°C) |
T2 (°C) |
Tf (°C) |
|Tf-T1|
(°C) |
|Tf-T2|
(°C) |
Q1=|Tf-T1|.M1 |
Q2=|Tf-T2|.M2 |
Q1/Q2
costante del rame |
| 250 |
250 |
70 |
24 |
67 |
3 |
43 |
750 |
10750 |
0,07 |
| 250 |
250 |
51 |
22 |
49 |
2 |
27 |
500 |
6750 |
0,07 |
| 200 |
200 |
71 |
23 |
66 |
5 |
43 |
1000 |
8600 |
0,11 |
| 250 |
500 |
81 |
24 |
73 |
8 |
49 |
2000 |
24500 |
0,08 |
| 250 |
200 |
70 |
23 |
66 |
4 |
43 |
1000 |
8600 |
0,12 |
| 150 |
250 |
77 |
24 |
72 |
5 |
48 |
750 |
12000 |
0,06 |
| 300 |
150 |
72 |
21 |
69 |
3 |
48 |
900 |
7200 |
0,12 |
Legenda:
Media delle
costanti del rame: 0,09
NOTA
dell'insegnante
Per Q1 e Q2 e costante non è stata volutamente inserita
l'unità di misura in quanto costituisce il risultato del lavoro. Attraverso discussione
verrà poi formalizzato il discorso.
CONCLUSIONI
Allora possiamo affermare che:
differenza1 x massa1 x costante della sostanza = differenza2 x massa2 x
costante della sostanza.
La temperatura finale di una mescolanza dipende da:
TEMPERATURE INIZIALI DELLE MASSE
MASSE DELLE SOSTANZE SCELTE
TIPO DI SOSTANZA SCELTA
STORIA DELL'ESPERIMENTO
L’esperimento non è stato lineare e semplice come ve lo presentiamo; ecco alcuni
stralci delle difficoltà.
Studente: facciamo il prodotto dell'acqua/prodotto del rame e troviamo il numero
che rappresenta la costante che stiamo cercando.
Ad esempio:
massa rame: 32g
massa acqua: 250 g
T rame: 23°C
T acqua: 81°C
Tfinale: 77°C
Calcolo: 32 x54 =1728 e 250 x 4 =1000
Prof.: i due prodotti non sono uguali. Come mai?
studenti : dipende dal rame calcoliamo 1000 / 1728 e troviamo la costante del rame =
0,57?. Proviamo più volte e se si ripete il valore possiamo dire di aver trovato la
costante del rame.
Date le nostre previsioni ci attendevamo un certo risultato più o meno costante
e qualcuno di noi era andato a cercare su testi e cercava di trovare un numero come 0,09 .
Inoltre la prof. ci ricorda che si tratta di un metallo e noi abbiamo visto che i
metalli sono dei buoni conduttori, quindi pensiamo che il fabbisogno di calore del rame
per ogni grammo sia basso.
Tabella dei dati relativi alla sostanza rame non trattato col calore: esperimento che
non ha fornito i dati previsti.
Confrontando i dati sperimentali trovati, che qui riportiamo:
M1
(g) |
M2
(g) |
T1
(°C) |
T2
(°C) |
Tf
(°C) |
|Tf-T1|
(°C) |
|Tf-T2|
(°C) |
Q1=|Tf-T1|.M1 |
Q2=|Tf-T2|.M2 |
Q2/Q1
costante del rame |
32 |
250 |
23 |
81 |
77 |
54 |
4 |
1728 |
1000 |
0,57 |
32 |
100 |
23 |
75 |
64 |
41 |
11 |
1312 |
1100 |
0,8 |
si è rilevato una grande differenza con le previsioni, e soprattutto non erano
costanti.
Osservazioni
L’esperimento del rame, non ha subito ottenuto i risultati previsti.
All’inizio non riuscivamo a capire il nostro errore e abbiamo pensato che
dipendesse dal rame.
Abbiamo provato con l'alcol denaturato e la costante si trovava!
Ma allora il nostro rame ha qualcosa che non va.
Per verificare le nostre ipotesi abbiamo messo il rame sulla fiamma , perché temevamo
che non fosse una sostanza pura.
Abbiamo poi ottenuto i risultati elencati nella prima tabella.
torna al piano di lavoro